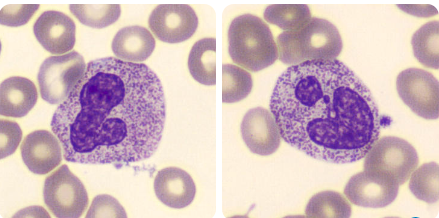
Os reticulócitos são uma das células precursoras das hemácias que desempenham um papel essencial na avaliação da eritropoiese, especialmente no contexto das anemias. Eles representam a última fase antes da maturação dos eritrócitos e são produzidos na medula óssea. Após entrarem na circulação, completam sua diferenciação em 1 a 2 dias.
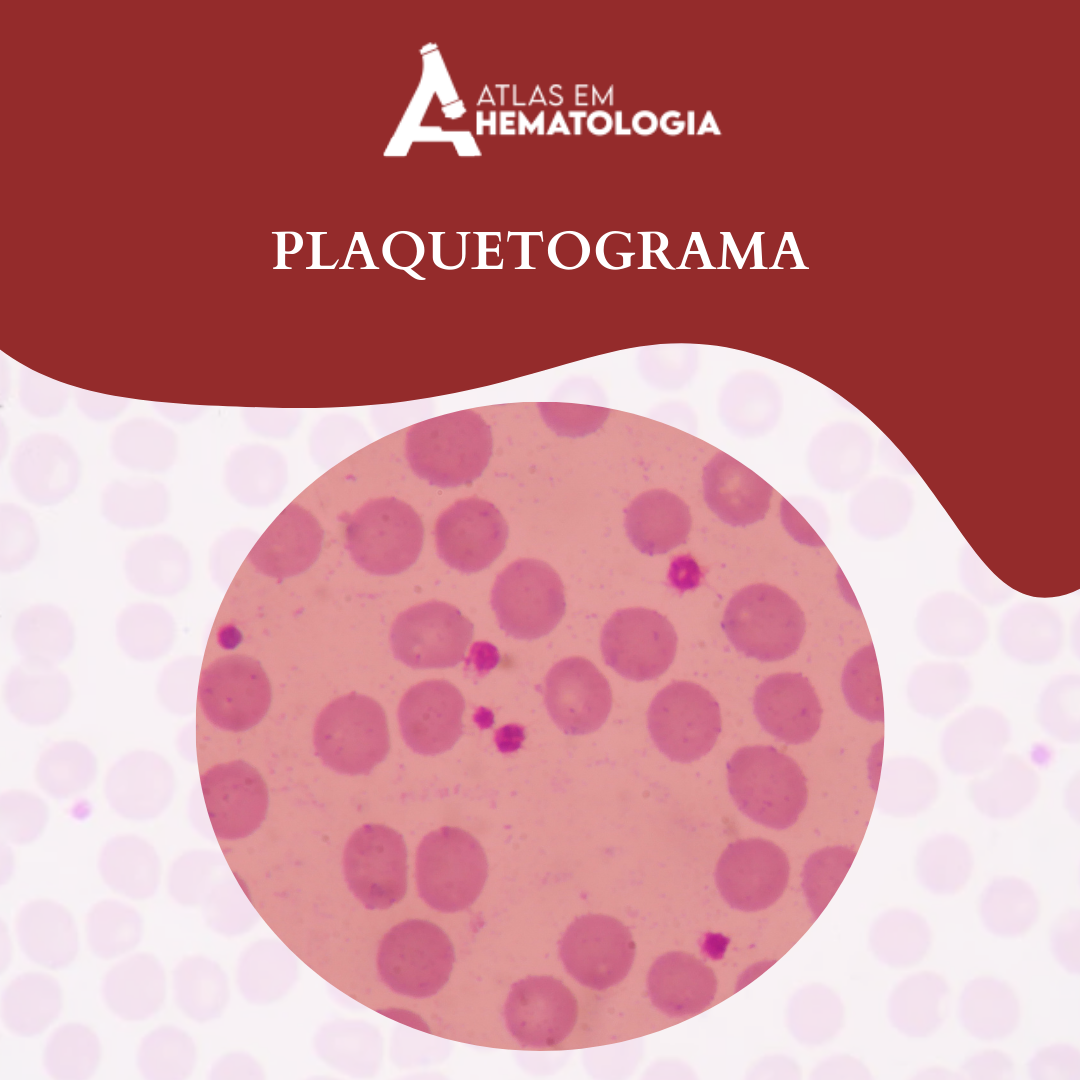
Por ainda conterem resíduos de RNA ribossômico, os reticulócitos apresentam coloração azulada característica, chamada policromasia (Quando em colorações hematológicas de rotina), estes achados podem ser melhor evidenciados em colorações especiais, como o Azul de Cresil Brilhante. A presença dessas células no sangue periférico reflete a atividade de produção de novas hemácias, tornando os reticulócitos um marcador valioso para compreender a resposta da medula óssea frente à anemia, ou mesmo a resposta ao tratamento.
Fonte: Laboratório de Hematologia – teorias, técnicas e atlas, 2020
Importância da contagem de reticulócitos nas anemias:
A contagem de reticulócitos é um exame bastante utilizado na investigação das anemias, pois permite avaliar a resposta da medula óssea na produção de novas hemácias. Esse exame auxilia na diferenciação entre anemias hipoproliferativas e regenerativas e é uma ferramenta valiosa para monitorar tratamentos, principalmente das anemias carenciais (tem resposta rápida), como a ferropriva (reposição de ferro) e megaloblástica (vitamina B12), além de avaliar a recuperação da eritropoiese após hemorragias e hemólise.
- Aumento dos reticulócitos: Indica uma resposta eritropoiética ativa, como ocorre em anemias hemolíticas, sangramentos agudos e recuperação de anemias ferropriva ou megaloblástica após reposição de nutrientes;
- Diminuição dos reticulócitos: Sinaliza uma falha medular, comum em anemias aplásticas e nas fases iniciais das anemias ferropriva e megaloblástica, antes da adequada reposição de ferro ou vitaminas essenciais.
Técnica de coloração azul de cresil brilhante (Exemplo):
Para a correta identificação dos reticulócitos, principalmente em quadros de anemia regenerativa, utiliza-se a coloração com azul de cresil brilhante. Esse método permite visualizar o RNA residual, garantindo maior precisão na contagem. O procedimento consiste em:
- Misturar 50 µL de sangue total (EDTA) com 50 µL de corante azul de cresil brilhante em um tubo de hemólise;
- Homogeneizar a amostra e incubar em banho-maria a 37°C por 15 minutos;
- Após a incubação, homogeneizar novamente, preparar o esfregaço na lâmina e deixar secar;
- Analisar em microscópio óptico com objetiva de imersão (1000X) e realizar a contagem.
Fonte: Laboratório de Hematologia – teorias, técnicas e atlas, 2020.
Cálculo da contagem de reticulócitos:
A contagem de reticulócitos é realizada analisando 1.000 hemácias no microscópio, geralmente distribuídas em cerca de cinco campos contendo aproximadamente 200 células cada. O número de campos analisados pode variar dependendo da condição clínica do paciente.
Os principais cálculos utilizados na interpretação podem incluir:
- Percentual de reticulócitos = (Número de reticulócitos contados / 1000) × 100;
- Contagem corrigida de reticulócitos (CCR) = Percentual de reticulócitos × (Hematócrito do paciente / Hematócrito padrão). Uso para hematócritos diminuídos;
- Índice de produção de reticulócitos (IPR) = CCR / Tempo de maturação dos reticulócitos.
Para calcular a CCR, considera-se um hematócrito padrão de 45% para homens adultos e 40% para mulheres adultas, adolescentes e crianças. Esses valores ajudam a avaliar se a produção de glóbulos vermelhos está adequada.
Entretanto, em casos de anemia grave, os reticulócitos podem permanecer mais tempo na circulação, exigindo um ajuste pelo tempo de maturação dos reticulócitos. Quanto mais baixo o hematócrito, maior o tempo necessário para os reticulócitos amadurecerem completamente.
Fonte: Hematologia laboratorial: teoria e procedimentos, 2016.
Esse ajuste é essencial para o cálculo do IPR, que reflete se a medula óssea está respondendo adequadamente à necessidade de novas hemácias.
Exemplo prático:
Uma paciente mulher adulta apresenta um hematócrito de 30% e um percentual de reticulócitos de 5%. Aplicando os cálculos:
CCR = 5% × (30% / 40%) → CCR = 5 × 0,75 = 3,75%
O tempo de maturação esperado para um hematócrito de 30% é de 2 dias.
IPR = 3,75 / 2 = 1,87
→ Um IPR acima de 3 indica uma resposta medular adequada, enquanto valores menores podem sugerir falha na produção de hemácias. No caso da paciente, o IPR de 1,87 sugere que a medula óssea ainda não está compensando totalmente a anemia, sendo necessária uma investigação adicional.
A IMPORTÂNCIA DA CAPACITAÇÃO PARA PROFISSIONAIS DA ÁREA LABORATORIAL
Se você busca aprofundar seus conhecimentos sobre anisocitose e outras condições hematológicas, além de aprimorar suas habilidades analíticas, investir em uma pós-graduação é uma excelente opção.
A Pós-graduação em Hematologia Laboratorial e Clínica foi desenvolvida para profissionais que desejam se destacar no mercado, com um conteúdo atualizado e voltado para a prática. Oferecemos aulas 100% online e ao vivo, com flexibilidade para conciliar com sua rotina. Nosso corpo docente é formado por especialistas renomados, referências nas suas áreas de atuação, garantindo uma formação de excelência.
Com uma metodologia que integra teoria e prática, o curso proporciona uma imersão completa na rotina laboratorial, preparando você para ser uma referência no campo da hematologia.
No Instituto Nacional de Medicina Laboratorial, nosso compromisso é transformar você em um profissional altamente capacitado.
Toque no botão abaixo e conheça a pós-graduação em Hematologia Laboratorial e Clínica.
Referências:
SILVEIRA, Cristina Magalhães da. Laboratório de Hematologia: teorias, técnicas e atlas. Editora Rubio, 2020.
SILVA, Paulo Henrique da et al. Hematologia laboratorial: teoria e procedimentos. Artmed, 2016.
ZAGO, M. A.; FALCÃO, R. P.; PASQUINI, R. Tratado de hematologia. Atheneu, 2013.