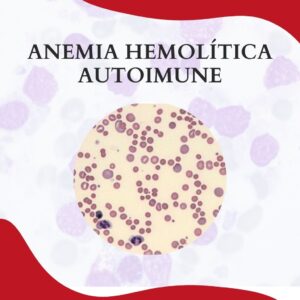
ANEMIA HEMOLÍTICA AUTOIMUNE POR ANTICORPOS FRIOS E QUENTES
Leitura: 5 min
A hemólise dos eritrócitos devido à ação de anticorpos contra sua membrana, é uma das principais causas de anemia hemolítica por fatores internos aos próprios glóbulos vermelhos, denominada anemia hemolítica autoimune (AHAI). A produção anormal […]